数据显示47.0%的人群对内分泌调理感兴趣,且64.3%已做过激素检査。性欲低下(45.9% 和性抗 拒(36.8% 是激素衰老的最直接体感,机构应将...
2026-05-06 31 医药医疗器械行业报告
临床研究通过对新药进行广泛的人体试验,评估其对疾病治疗的有效性以 及对人体的安全影响。候选药物临床前研究完成并经临床试验申请批准(IND) 后即可进行临床试验。临床试验按阶段主要分为 I-IV 期,其中 I、II、III 期在 新药在批准上市前进行,而 IV 期临床试验通常在新药注册申请(NDA)完成, 药品上市后进行。 不同临床阶段试验标准和受试人群数量存在较大差异。IND 审核主要关注 候选药物化学结构及其作用机理、副作用、生产工艺和稳定性等。临床 I 期通 过试验,评估候选药物在人体的药理学及安全性。这一阶段通常需要 20-30 例 受试者,规模较小。到临床 II 期验证药物治疗作用和安全性阶段,受试人群增 加到几十至几百人不等,规模扩大,对研发机构临床招募能力提出较高要求。 临床 III 期阶段,主要关注药物用法用量及风险收益比,这一阶段临床受试人 群扩展到几百到数千人。完成临床 III 期后即进入 NDA 阶段,药品上市后仍会 进行临床 IV 期考察在广泛使用条件下的药物疗效和不良反应。
横向来看,临床 CRO 较临床前 CRO 有更为明显的人员规模效应。临床前 CRO 企业更多的是依赖于企业建立的技术平台数量,每个人可参与的环节有 限,因而临床前 CRO 人均创收及人均创造净利润与企业规模相关性较弱。例 如临床前 CRO 领域龙头企业药明康德,人员规模在 2 万人以上,为康龙化成 规模的 3 倍以上,但人均创收和人均创利甚至略低于康龙化成。而对于临床 CRO 企业,企业规模越大,每个人可参与的外包服务环节以及临床中心实验 室越多,单项目成本相应下降,从而形成项目数量和人员投入的正向循环,企 业规模效应凸显。以同为临床 CRO 的博济医药和泰格医药为例,泰格医药人 员数量远高于博济医药,相应的,泰格医药人均创收和人均创利分别为博济医 药的 10 倍。
CMO/CDMO 按阶段可分为实验室(临床前)和工厂(商业化)两大阶段。 药企把生产工艺优化及商业化大规模生产交给 CMO/CDMO 企业后,集中资源 与精力在研发环节,提升药物研发、生产整体成功率和效率。其中,CMO (Contract Manufacture Organization)为药企提供产品研发阶段定制化的原料 药、中间体、制剂等服务,提高新药生产效率。CDMO(Contract Development Manufacture Organization)在 CMO 基础上为药企优化技术路线。CMO/CDMO 按进程分为实验室和工厂扩产阶段,不同生产环节除产出药品外,还会设置不 同的工艺改进、制剂生产优化目标。

标签: 医药医疗器械行业报告
相关文章

数据显示47.0%的人群对内分泌调理感兴趣,且64.3%已做过激素检査。性欲低下(45.9% 和性抗 拒(36.8% 是激素衰老的最直接体感,机构应将...
2026-05-06 31 医药医疗器械行业报告

针对2612名国内18-35岁的青年调研结果显示,超过八成的青年表示对于性健康知识非常了解或比较了解。显示在文化多元的氛围下,青年 的性健康意识逐渐成...
2026-05-06 28 医药医疗器械行业报告
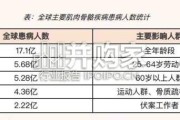
作为深耕中医药健康领域的民族企业,花红药业始终秉持“守护公众肌骨健康”的初心。我们深切体察到广大患者对于“安全止痛、便捷康复”的迫切期待,同时也关注到...
2026-05-06 21 医药医疗器械行业报告
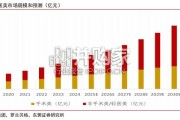
中国轻医美赛道有望成为推动行业增长的重要动力。中国医疗美容市场近年来保持较快 扩张,其中轻医美项目增长显著快于手术类项目。根据美团、罗兰贝格数据,20...
2026-05-06 19 医药医疗器械行业报告

伴随着医美产业的发展,医美注射类产品日益得 到市场关注,发展至今已经有多款产品上市并获 得市场认可,以玻尿酸、胶原蛋白、再生制剂、 肉毒素、外泌体等为...
2026-05-06 18 医药医疗器械行业报告

根据《中国卫生健康统计年鉴2022》和国家统计 局数字推算,2021年中国影像科医生配置约为 0.17人/千人,且地区分配严重不均;同时,患者 数量增...
2026-05-05 30 医药医疗器械行业报告
最新留言