由于目前缺乏直接针对肝纤维化的化学药和生物药,若考虑针对病因治疗药物如干扰素、核苷类药 物,Data Bridge预计到2029年全球相关药物市场规模...
2025-01-19 2 医药医疗器械行业报告
评价流程:确定参比制剂与开展BE试验是两大关键。开展仿制药质量和疗效一致性评价工作,要求已经批准上市的仿制药品, 在质量和疗效上与原研药品能够一致,临床上与原研药品可以相互替代。
评价时间: 单个品种通过一致性评价周期约为20-28个月。单个品种通过一致性评价的周期约为20-28个月,其中:①确定并获得参比制剂需1-3个月;②开展药学一致性评价需6-12个月;③开展BE试验需7 月左右(从BE备案至试验终止);④申报受理和审评审批需6个月左右。
标签: 医药医疗器械行业报告
相关文章

由于目前缺乏直接针对肝纤维化的化学药和生物药,若考虑针对病因治疗药物如干扰素、核苷类药 物,Data Bridge预计到2029年全球相关药物市场规模...
2025-01-19 2 医药医疗器械行业报告
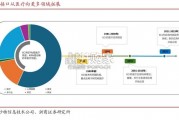
脑机接口的早期应用集中于医疗健康领域,最初旨在为运动障碍患者提供新型辅助技 术。随着 BCI 技术的进步,脑机接口逐渐扩散至心理健康、智能家居、虚拟现...
2025-01-16 101 医药医疗器械行业报告

中药NDA流程主要为:药审中心承办-进入新报任务(平均240天,包含统计/药理毒理/临床/药学/合规等任务 -1至2个月-进入补充资料任务 (平均60...
2025-01-13 78 医药医疗器械行业报告

目前,医用同位素的生产主要靠研究堆、回旋加速器生产制备。截止 2023 年底,全球可用于生产医用同位素的研究堆堆不到 80 座,制备放射性药物的 回旋...
2025-01-09 62 医药医疗器械行业报告

锥形束 CT(CBCT)目前主要应用于口腔诊疗领域,国产化率已经 达到较高水平。从应用场景来看,锥形束 CT 设备在口腔诊疗领域的 使用场景非常广泛,...
2025-01-07 72 医药医疗器械行业报告
最新留言