2022年全球肝癌新发病例86.5万,死亡75.8万,死亡/发病比高达87.6%。中国新发病 例36.8万,占全球42.5%。东亚贡献全球近半数病例,...
2026-05-12 29 医药医疗器械行业报告
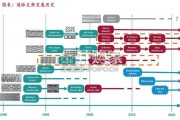
中药NDA流程主要为:药审中心承办-进入新报任务(平均240天,包含统计/药理毒理/临床/药学/合规等任务)-1至2个月-进入补充资料任务 (平均60天,任务内容和新报一致)-国家/地方药监局审批-NMPA签发药品批件,离开补充资料任务后需要约15天被批准生产。 从已上市药品的时间轴来看,总历时集中在一年,最低为286天,最多为522天,历时更长的导致因素主要为补充资料任务时间和任务之间的 间隔时间。申报时间较后的新药,补充任务时间有拉长趋势。整体历时仍然变化不大。

标签: 医药医疗器械行业报告
相关文章
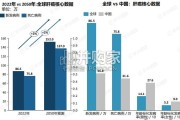
2022年全球肝癌新发病例86.5万,死亡75.8万,死亡/发病比高达87.6%。中国新发病 例36.8万,占全球42.5%。东亚贡献全球近半数病例,...
2026-05-12 29 医药医疗器械行业报告

心理健康正日益成为我国健康战略的关键一环。最新统计显示,国内线上心理咨询覆盖率已达32.7%,较前年增长8.3个百分点,反映出公众心理支持需求的不断增...
2026-05-11 36 医药医疗器械行业报告
心脏介入:从影像到治疗,全线布局。其中AGENT DCB球囊是美国首款/唯一治疗ISR的冠脉药球;AVVIGO+血管内超声,行业先驱,产品升级后竞争...
2026-05-10 44 医药医疗器械行业报告

展望未来十年,中国医药创新正站在新的分水岭 上。决定其能否实现新一轮跃迁的关键,在于效率能 否转化为被全球认可和定价的创新价值。从“效率高 地”迈向“...
2026-05-09 39 医药医疗器械行业报告

数据显示47.0%的人群对内分泌调理感兴趣,且64.3%已做过激素检査。性欲低下(45.9% 和性抗 拒(36.8% 是激素衰老的最直接体感,机构应将...
2026-05-06 59 医药医疗器械行业报告

针对2612名国内18-35岁的青年调研结果显示,超过八成的青年表示对于性健康知识非常了解或比较了解。显示在文化多元的氛围下,青年 的性健康意识逐渐成...
2026-05-06 50 医药医疗器械行业报告
最新留言