由于目前缺乏直接针对肝纤维化的化学药和生物药,若考虑针对病因治疗药物如干扰素、核苷类药 物,Data Bridge预计到2029年全球相关药物市场规模...
2025-01-19 2 医药医疗器械行业报告
新药研发热情高涨。新药研发是医药行业永恒的主题,也是行业和制药公司发展的根本动力。2000 年以来,每年在研新药的数量持续上升,屡创新高,2017 年达到 1.5 万,是 2001 年的 2.5 倍。
应对现有产品专利到期的被动选择:纵观国际重磅药物的历史销售数据可以发现,新药在专利到期以后通常会由于仿制药的竞争,销售额发生断崖式下降,且销售额峰值越高的药物出现这种现象就越明显,如辉瑞用于高胆固醇血症治疗的药物——立普妥,销售峰值高达 120 多亿美元,目前的销售额仅剩 20 亿美元。因此,为了避免新药专利到期对公司业绩带来的巨大冲击,药企只能通过不断的自主研发或收购新药项目来丰富自身的新药产品线,以抵抗业绩的急剧下滑。
一致性评价政策落地,仿制药临床研发外包需求集中爆发:根据一致性评价政策的规定,(1)国家基药(2012 年版)中 2007 年 10 月 1 日前批准上市的化学药品仿制药的口服固体制剂,应在 2018 年底前完成一致性评价。据此粗略统计,理论上到 2018 年底将有共计 289 个品种的19715 个批文需要完成一致性评价,共涉及 2028 个企业。(2)化学药品新注册分类实施前批准上市的其他仿制药,自首家品种评价完成后,其他家相同品种应在 3 年内完成,逾期未完成的,均不予再注册。(3)同品种药品通过一致性评价的生产企业达到 3 家以上的,在药品集中采购等方面不再选用未通过一致性评价的品种。因此,在政策落地后的短短几年时间里,大量已上市的仿制药需要重新进行并完成一致性评价,时间紧、任务重,因此将这部分工作外包给专业的公司和团队去负责就成了必然的选择。此外,未来仿制药在获批上市之前均需要通过一致性评价,这也为医药合同外包服务行业提供了新的市场需求。

标签: 医药医疗器械行业报告
相关文章

由于目前缺乏直接针对肝纤维化的化学药和生物药,若考虑针对病因治疗药物如干扰素、核苷类药 物,Data Bridge预计到2029年全球相关药物市场规模...
2025-01-19 2 医药医疗器械行业报告
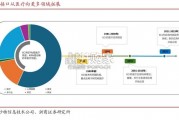
脑机接口的早期应用集中于医疗健康领域,最初旨在为运动障碍患者提供新型辅助技 术。随着 BCI 技术的进步,脑机接口逐渐扩散至心理健康、智能家居、虚拟现...
2025-01-16 101 医药医疗器械行业报告

中药NDA流程主要为:药审中心承办-进入新报任务(平均240天,包含统计/药理毒理/临床/药学/合规等任务 -1至2个月-进入补充资料任务 (平均60...
2025-01-13 78 医药医疗器械行业报告

目前,医用同位素的生产主要靠研究堆、回旋加速器生产制备。截止 2023 年底,全球可用于生产医用同位素的研究堆堆不到 80 座,制备放射性药物的 回旋...
2025-01-09 62 医药医疗器械行业报告

锥形束 CT(CBCT)目前主要应用于口腔诊疗领域,国产化率已经 达到较高水平。从应用场景来看,锥形束 CT 设备在口腔诊疗领域的 使用场景非常广泛,...
2025-01-07 72 医药医疗器械行业报告
最新留言