由于目前缺乏直接针对肝纤维化的化学药和生物药,若考虑针对病因治疗药物如干扰素、核苷类药 物,Data Bridge预计到2029年全球相关药物市场规模...
2025-01-19 2 医药医疗器械行业报告
吸入制剂的疗效取决于肺部的沉积量,较理想的颗粒直径为1-5μm。吸入制剂粒子大小在肺部沉降中扮演着重要的角色。若粒子直径小于 1μm,有很高的成分比例被呼出;介于1-5μm时可以达到肺的周边;大于5μm以上时,粒子沉降的位置就会从肺的周边移至传导性气道中; 超过10μm,则沉积于口咽的比例就会增多;10-15μm的粒子容易沉降于鼻腔和咽部。 不同装置类型药物沉积于肺中的比率不尽相同,大部分的气雾吸入系统沉积于肺中的比率约为1-50%。药物沉积量取决于装置类型、病人本 身、药物种类、疾病类型等,除了沉积在肺部以外,会有口咽损失,装置残留损失,和呼气/环境损失等。如Albuterol在pMDI加压定量吸入器 两个喷雾计量200微克药物中,约有20-40微克到达肺部,其余部分在口咽、设备、周围环境中或随呼出的气体排出。 相同药物的不同吸入装置正确使用时具有临床效果等效性。不同的装置不仅肺部沉积不同,肺部给药的名义剂量也不同,但是《chest》期刊 上证明按照正确的使用方法,临床效果等同。以支气管扩张剂Ipratropium为例,SVN的名义剂量较高为0.5mg,而pMDI仅需0.04mg,SVN小 容量喷雾器的名义剂量比pMDI压力定量吸入器多约12倍,按要求使用pMDI或SVN上标示的剂量,可以达到相同的临床效果。
单独使用经典药动学研究不足以评价吸入制剂的生物等效性。局部作用的吸入制剂给药后,首先在呼吸道发挥作用,然后 才进入全身血液循环。如沙美特罗替卡松粉雾剂,吸入后作用于支气管和肺部,而后通过肺泡吸收进入到血液循环中。给 药后在靶组织中的浓度与血药浓度是不同步的,其药动学和效应/毒性器官暴露量之间缺乏相关性,经典药动学研究在吸入 制剂上确实有局限性,需要建立一套新的体系来评估这些吸入仿制药的生物等效性。 美国FDA和欧盟EMA等效性评价标准不同。为了开发安全有效的药物,美国FDA 于20世纪90年代中期提出了集合证据加权 法( weight-of-evidence approach) 来综合评价吸入制剂的全身吸收量和效应 /毒性器官生物等效性,主要包括 :①体外研究; ②药动学研究;③药效学或临床终点研究。FDA 已明确要求首先采用群体生物等效性方法进行体外研究,结合药动学指标 和临床终点指标共同评价仿制制剂的安全性和有效性,吸入仿制药的BE具体是处方和装置相似、体外试验相同、全身暴露 等同以及PD/临床疗效等同等四项全部满足要求后才能确定最终的生物等效性。欧盟EMA要求相对宽松,生物等效性BE通 过条件更多。在体外等同的情况下,不需要做太多的验证试验,只需要满足药学等同或全身暴露等同或PD安全性等同其中 一项就可以确定BE。相信随着装置研究的不断进步,吸入给药的长期安全及生物等效评价会更加完善。

标签: 医药医疗器械行业报告
相关文章

由于目前缺乏直接针对肝纤维化的化学药和生物药,若考虑针对病因治疗药物如干扰素、核苷类药 物,Data Bridge预计到2029年全球相关药物市场规模...
2025-01-19 2 医药医疗器械行业报告
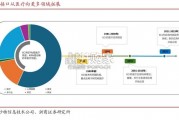
脑机接口的早期应用集中于医疗健康领域,最初旨在为运动障碍患者提供新型辅助技 术。随着 BCI 技术的进步,脑机接口逐渐扩散至心理健康、智能家居、虚拟现...
2025-01-16 101 医药医疗器械行业报告

中药NDA流程主要为:药审中心承办-进入新报任务(平均240天,包含统计/药理毒理/临床/药学/合规等任务 -1至2个月-进入补充资料任务 (平均60...
2025-01-13 78 医药医疗器械行业报告

目前,医用同位素的生产主要靠研究堆、回旋加速器生产制备。截止 2023 年底,全球可用于生产医用同位素的研究堆堆不到 80 座,制备放射性药物的 回旋...
2025-01-09 62 医药医疗器械行业报告

锥形束 CT(CBCT)目前主要应用于口腔诊疗领域,国产化率已经 达到较高水平。从应用场景来看,锥形束 CT 设备在口腔诊疗领域的 使用场景非常广泛,...
2025-01-07 72 医药医疗器械行业报告
最新留言