大模型的推理能力和多模态能力持续升级、应用成本不断下降,驱动医疗机构加 速融合 AI 技术。根据 DataBridge 的测算,预计至 2031 年全...
2025-04-19 16 医药医疗器械行业报告
注射后 7 天内,两项试验的 320 位参与者中有 48 位(15.0%) 报告了不良反应。具体来说,在低剂量,中剂量,高剂量和明矾中, 报告不良反应的参与者的数量分别为 5(20.8%),4(16.7%),6 (25.0%)和 3(12.5%)。最常见的不良反应是注射部位疼痛(I 期出现 14 例,II 期出现 21 例),以及发烧(I 期出现 2 例,II 期出 现 8 例)。所有不良反应均为轻度(1 级或 2 级),短暂且具有自限 性,不需要任何治疗,安全性较好。 对 COVID-19 疫苗的关注之一是抗体依赖性增强(ADE)现象 ADE 是指有些与病毒结合的特异性抗体,在结合病毒之后,不但没 有起到中和的效果,反而为病毒入侵细胞提供了新途径。这是因为, 病毒需要通过和细胞上的特定受体结合从而入侵细胞,若细胞不表 达相应受体,病毒则无法入侵宿主细胞。然而,当抗体与病毒结合 后,抗体的 Fc 端可以与细胞上的 Fc 受体相结合,介导病毒/抗体复 合物进入细胞。这个效应可能增加病毒的传染性和烈度。因此,在 接种疫苗后,存在可能会出现提高人们感染病毒的几率或受到感染 后疾病的严重性的风险。ADE 现象已被报道在 MERS 冠状病毒疫 苗和 SARS 冠状病毒疫苗的研究中出现。然而,目前未在临床中及 临床前研究中观察到该现象。此外,与全灭活病毒有关的另一个问 题,是与疫苗相关的增强呼吸道疾病(VAERD)。
此前,康希诺生物公布了重组新型冠状病毒疫苗 (Ad5-nCoV) II 期临床试验研究结果。Ad5-nCoV 疫苗是一种表达 SARS-CoV-2 刺突糖蛋白(S 蛋白)的复制缺陷 Ad5 载体疫苗。此次公布的数据 来自一项随机,双盲,安慰剂(仅包含疫苗赋形剂,没有病毒颗粒) 对照的 II 期临床试验,共招募了 508 名 HIV 阴性且未曾感染过 SARS-CoV-2 的健康成年人,平均年龄为 39.7 岁(范围 18—83 岁)。 受试者被随机分配到 1x1011病毒颗粒剂量组、5x1010病毒颗粒剂量 组以及安慰剂组,仅注射一针。此次临床试验中,研究者分别在疫苗接种后的第 14 天和第 28 天对受试者的抗 RBD(新冠病毒 S 蛋白受体结合区域)特异性抗体 水平、活病毒中和抗体水平和假病毒中和抗体水平 3 项指标进行检 测。结果显示,疫苗接种后,受试者体内几项抗体水平相比安慰剂 组均有显著提升,显示出一定保护作用。对于腺病毒载体疫苗,最主要的缺点是人群普遍存在针对常见 的人血清型腺病毒的中和抗体,而机体对载体的应答可能会干扰对 疫苗抗原的免疫应答,干扰疫苗免疫效果。从检测情况来看,此次 508 名参与者中,有 266 名(52%)对 Ad5 载体具有较高的既存免 疫力(抗体滴度≥200)。根据此前研究,全球既存 Ad5 抗体的成年 人占比较大,比例超过 1:200。此次临床试验参与者的抗 Ad5 基 线免疫力基本代表了中国成年人。

标签: 医药医疗器械行业报告
相关文章

大模型的推理能力和多模态能力持续升级、应用成本不断下降,驱动医疗机构加 速融合 AI 技术。根据 DataBridge 的测算,预计至 2031 年全...
2025-04-19 16 医药医疗器械行业报告
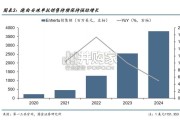
复盘目前增长:2024 自然年第一三共 HER2 ADC 德曲妥珠单抗在全球销售额合约 38 亿美 元,同比增长约 50%,德曲妥珠单抗强劲增长得益于...
2025-04-18 29 医药医疗器械行业报告

世界卫生组织提出“健康不仅是躯体没有疾病,还要具备心理健康、社会适应良好和有道德”。2025年,国民对健康的定义 除了身心健康、状态积极、作息规律之外...
2025-04-17 35 医药医疗器械行业报告
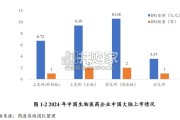
根据药渡数据库统计,在 2024 年中,总计 19 家中国生物医药公司在中国大陆、 香港和美国纳斯达克完成 IPO。其中 A 股上市 6 家(科创板上...
2025-04-17 32 医药医疗器械行业报告

在当今全球化竞争日益激烈与国内经济结构深刻转型的背景下,企业面临着前所未有的复杂外部环境。高 管作为企业战略实施与日常运营的核心驱动力,其团队的稳定与...
2025-04-17 22 医药医疗器械行业报告

2021 年,中美关节置换手术量差距仍然巨大,2021 年中国全髋关节置换 术共约 77 万例,全膝关节置换术共约 52 万例,而美国 2021 年全...
2025-04-16 26 医药医疗器械行业报告
最新留言