数据显示47.0%的人群对内分泌调理感兴趣,且64.3%已做过激素检査。性欲低下(45.9% 和性抗 拒(36.8% 是激素衰老的最直接体感,机构应将...
2026-05-06 40 医药医疗器械行业报告
三代疫苗技术趋于成熟,在新冠研发品种中占比50%:三代疫苗技术从2003年开始在以往的流行性疾病上尝试研发,到2015年前后在寨卡病毒、埃博 拉病毒、流感疫苗研发中广泛使用,十余年的尝试促进了三代技术的成熟。在新冠疫情突然爆发的局面下,病毒载体疫苗、DNA疫苗、RNA疫苗的三 代疫苗技术平台集体亮相,当前临床和临床前阶段品种占比都接近50%。mRNA疫苗技术更是后来居上,率先披露三期保护率初步数据,已临近顺利 获批的关键节点。病毒载体疫苗是唯一获批过的的三代疫苗技术,是当前疫苗技术升级的重点方向之一,候选的病毒载体和相应的疫苗品种在不断的丰富。衡量病毒载 体质量的主要标准:插入基因序列在病毒基因组上的稳定性;诱导免疫反应的能力;安全性;大规模生产的潜力。当前已经有人类腺病毒、痘病毒、 麻疹病毒等应用到疫苗研发中,目前在研的病毒载体疫苗品类广泛,针对埃博拉病毒的腺病毒载体和rVSV载体疫苗已经获批,新冠品种中包含多种病 毒载体平台。病毒载体技术在2014年西非爆发埃博拉病毒疫情引发的研发热潮中广泛使用并首次有产品获批。2019年11月11日,默沙东rVSV-ZEBOV获欧洲药物 管理局(EMA)有条件批准上市;2019年12月20日,获美国FDA批准上市,品牌名为ERVEBO®,用于18岁及以上人群的主动免疫,以预防由扎伊 尔型埃博拉病毒引起的埃博拉病毒病。2020年2月14日,包括刚果民主共和国(DRC)在内的四个非洲国家已经批准了ERVEBO。其中在几内亚完成的 临床三期实验数据显示ERVEBO保护率达100%。 Ad5-EBOV由中国人民解放军军事医学研究院生物工程研究所和康希诺生物股份公司共同研发,是一种5型腺病毒载体埃博拉病毒病疫苗。该疫苗于 2017年10月获得中国新药申请批准,注册分类为1类预防用生物制品,已申请作为应急使用及国家储备,是我国第一款获批的埃博拉疫苗。 二期临床结 果显示,在安全性良好的前提下,疫苗的抗体阳转率达96%。
俄罗斯的gamaleya研究所针对埃博拉病毒开发2剂的rVSV/Ad5 GamEvac联合疫苗,在临床一期和临床二期未见疫苗相关严重不良反应,现已在俄罗 斯获批上市并开展四期临床。 除了上述三种获批品种外,杨森制药的Ad26病毒载体品种Ad26.ZEBOV正在美国进行Ⅲ期临床试验。体液免疫:COV001是一项设盲、多中心、随机对照1/2期临床试验,共有1077例健康成人受试者参加,年龄18-55岁,并按剂量分为单次注射和28天第二 次注射,以脑膜炎球菌结合疫苗注射组作为对照。试验结果表明,在接受一剂ChAdOx1 nCoV-19接种的志愿者中,与针对新冠病毒刺突蛋白的抗体水平在 接种后第28天达到峰值,在接种后56天仍然维持在高水平。在两次接种疫苗的志愿者中,针对S蛋白的抗体水平显著高于接种一次疫苗的志愿者。在接种 后1个月,91%的接种一剂疫苗的参与者和100%接受第二次接种的参与者中观察到了有效削弱新冠病毒活性的中和抗体。中和抗体水平与COVID-19康复期 患者相当。 细胞免疫:研究人员也使用了特异性干扰素γ酶联免疫斑点测定对志愿者的T细胞免疫反应进行了检测。检测结果表明,志愿者在接种疫苗后第7天就出现细 胞免疫反应,这一免疫反应在接种疫苗14天后达到峰值,并且在接种后第56天仍然维持在较高水平。安全性:ChAdOx1 nCoV-19组出现一次性局部和全身反应,与既往试验和其他腺病毒载体疫苗相当。包括暂时性注射部位疼痛和压痛、轻度至中度头痛、 疲乏、寒战、发热、不适和肌肉疼痛。试验未报告严重不良事件,使用预防性对乙酰氨基酚(一种止痛药)后反应减轻,第二次给药后不良事件发生频率 降低。此疫苗的2b/3期临床试验已经在英国、南非和巴西展开。在英国已经有4000名志愿者入组,预计将再注册1万名志愿者。在巴西进行的临床试验计划 注册5000名志愿者。

标签: 医药医疗器械行业报告
相关文章

数据显示47.0%的人群对内分泌调理感兴趣,且64.3%已做过激素检査。性欲低下(45.9% 和性抗 拒(36.8% 是激素衰老的最直接体感,机构应将...
2026-05-06 40 医药医疗器械行业报告

针对2612名国内18-35岁的青年调研结果显示,超过八成的青年表示对于性健康知识非常了解或比较了解。显示在文化多元的氛围下,青年 的性健康意识逐渐成...
2026-05-06 37 医药医疗器械行业报告
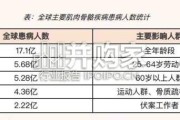
作为深耕中医药健康领域的民族企业,花红药业始终秉持“守护公众肌骨健康”的初心。我们深切体察到广大患者对于“安全止痛、便捷康复”的迫切期待,同时也关注到...
2026-05-06 24 医药医疗器械行业报告
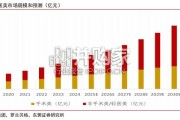
中国轻医美赛道有望成为推动行业增长的重要动力。中国医疗美容市场近年来保持较快 扩张,其中轻医美项目增长显著快于手术类项目。根据美团、罗兰贝格数据,20...
2026-05-06 21 医药医疗器械行业报告

伴随着医美产业的发展,医美注射类产品日益得 到市场关注,发展至今已经有多款产品上市并获 得市场认可,以玻尿酸、胶原蛋白、再生制剂、 肉毒素、外泌体等为...
2026-05-06 20 医药医疗器械行业报告

根据《中国卫生健康统计年鉴2022》和国家统计 局数字推算,2021年中国影像科医生配置约为 0.17人/千人,且地区分配严重不均;同时,患者 数量增...
2026-05-05 31 医药医疗器械行业报告
最新留言