本次调研显示,56.0%的受访者来自公立三甲医院,且85.1%为执业超过10年的资深医务人 员。这个样本特征非常关键,它意味着当前医疗AI的积极使用者...
2026-06-04 19 医药医疗器械行业报告
根据 PDB 数据库的样本数据,2012-2020 年样本医院注射剂销量同比增速与入院人数增 速高度相关,2012-2019 年注射剂销量 CAGR+2.4%,保持低速增长。2020 年受疫情影 响,20Q1 注射剂销量创单季度低点, 20Q2-Q4 同比均负增长但降幅逐季度收窄,21Q1 销量同比增长 21.5%,呈现快速恢复。由于注射剂 2020 年 5 月开始被纳入一致性评价, 在第四批和第五批国家集采中分别有 8 个/32 个注射剂产品被纳入。随着入院人数和终端药品需求的增长,我国药包材行业市场规模呈现稳定增长,其中药用 玻璃市场规模总体震荡攀升。根据中玻网统计,我国药用玻璃行业市场规模从 2012 年约 175 亿元增长到 2020 年的 234 亿元,CAGR+3.7%。自 2015 年中国药用玻璃市场突破 200 亿元后,持续稳定在 200 亿以上,2020 年药用玻璃市场规模 234 亿元,同比+2.6%。 我们预计随着注射剂纳入一致性评价和疫情影响逐渐消除,药用玻璃市场有望加快增长。
药品一致性评价和关联审批是推动药用玻璃包材行业升级的核心动力,药品集采加快助推。 从需求上看,药品一致性评价和关联审批两大政策本质上仍是为了提高药品安全性,而药 企为了顺利通过评价与审批,将使用中硼硅玻璃替换原有钠钙、低硼硅玻璃包材。从供给 上看,随着我国国内中硼硅玻璃技术的突破和生产的量产,我国国产中硼硅玻璃有望打破 外资企业的垄断,以更优的价格和质量实现国产药用玻璃的渗透提升。 仿制药一致性评价目的是对已经批准上市的仿制药,按与原研药品质量和疗效一致的原则, 进行质量一致性评价,即仿制药需在质量与药效上达到与原研药一致的水平。2017 年 12 月我国颁布《已上市化学仿制药(注射剂)一致性评价技术要求(征求意见稿)》,指出注射剂 使用的直接接触药品的包装材料和容器应符合总局颁布的包材标准,不建议使用低硼硅玻 璃和钠钙玻璃,该政策有助于推动药用玻璃向中硼硅玻璃替换升级。注射剂是目前化学仿制药中的重要组成部分,推动进行一致性评价有望加快拉动国内中硼 硅玻璃的需求。自 2020 年 5 月注射剂被正式纳入一致性评价以来,我国注射剂申请通过 一致性评价的品种和品规数量快速增加。截至 2021 年 7 月末,过去 15 个月我国累计通过 注射剂一致性评价 118 个品种、248 个品规。

标签: 医药医疗器械行业报告
相关文章

本次调研显示,56.0%的受访者来自公立三甲医院,且85.1%为执业超过10年的资深医务人 员。这个样本特征非常关键,它意味着当前医疗AI的积极使用者...
2026-06-04 19 医药医疗器械行业报告
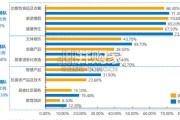
从需求结构看,当前银发消费已呈现出较为清晰的梯队化特征。根据中国老 龄协会专项调查,功能性食品及衣着、旅游度假、健康养生处于第一梯队, 文体娱乐、金融...
2026-06-04 30 医药医疗器械行业报告
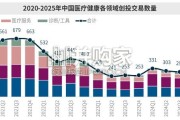
2025年中国医疗健康私募股权投资市场延续2024年的企稳态势,上半年小幅降温后,下半年受益于二级市场全面回暖,单季度融资数量快速回升至300笔以上。...
2026-06-01 35 医药医疗器械行业报告
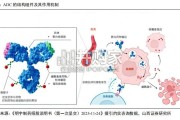
抗体药物偶联物(ADC)是一种靶向癌症疗法,融合了单克隆抗体的精准靶向能力与细 胞毒素的强效杀伤效力。传统的化疗是抗癌治疗的主要手段,但对癌细胞的选择...
2026-05-29 29 医药医疗器械行业报告

2025 年,药品注册申请申报量持续增长,药审中心受理各类注册 申请 20149 件(同比增加 3.00%,以受理号计,下同),包括药品制剂 注册申请...
2026-05-28 35 医药医疗器械行业报告
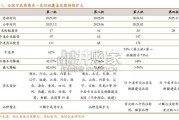
第四批全国中成药集采共纳入 28 个采购组、90 个产品,涉及活血止痛膏、 银杏叶提取物注射液、小儿肺热咳喘颗粒等临床常用品种,以及银丹心脑通软 胶囊...
2026-05-28 26 医药医疗器械行业报告
最新留言