数据显示47.0%的人群对内分泌调理感兴趣,且64.3%已做过激素检査。性欲低下(45.9% 和性抗 拒(36.8% 是激素衰老的最直接体感,机构应将...
2026-05-06 33 医药医疗器械行业报告
CGT治疗原理:将治疗性基因导入人体目标细胞,以纠正基因缺陷精准发挥治疗作用。当目的基因被导入到靶细胞内,它们或与宿主细胞染色体 整合成为宿主遗传物质的一部分,或不与染色体整合而位于染色体外,但都能在细胞中表达,起到治疗疾病的作用。DNA矫正:指将致病DNA链的异常碱基进行纠正,而正 常部分予以保留 DNA置换:是用正常DNA通过体内DNA同源重组,原位 替换病变细胞内的致病DNA,使细胞内的DNA完全恢复 正常状态 DNA增补:指将目的DNA导入病变细胞或其他细胞,不 去除异常DNA,而是通过目的DNA的非定点整合,使其 表达产物补偿缺陷DNA的功能或使原有的功能得到加强。 DNA治疗多采用此种方式。这种方法增补的是显性DNA 多用于治疗隐性病 DNA失活:早期一般是指反义核酸技术。它是将特定的反 义核酸,包括反义RNA,反义DNA和核酶导入细胞,在翻 译和转录水平阻断某些基因的异常表达。近年来又有反基 因策略、肽核酸、DNA去除和RNA干扰技术。FDA 定义基因治疗:基于修饰活细胞遗传物质而进行的医学干预。
细胞可以体外修饰,随后再注入患者体内,使细胞内发生遗传学改 变。这种遗传学操纵的目的可能会预防、治疗、治愈、诊断或缓解 人类疾病。自上世纪50年代DNA双螺旋被发现以来,基因概念深入人心。1990年,美国批准开展全球首例以逆转录病毒为载体的基因治疗临床试验。此后10年整个行业呈现欣 欣向荣的发展态势。但1999年,在一例腺病毒基因治疗中发生患者死亡事件,2002年两名SCIF患者治疗后获继发白血病,导致2003年FDA叫停所有逆转录病毒的临 床试验。2009年,宾夕法尼亚大学利用腺相关病毒载体成功治愈LCA患者,自此CGT重回大众视野。2012年, 腺相关病毒衍生的基因治疗药物 Glybera 首获EMA批 准上市, 开启基因治疗新时代。2016年, EMA批准第二款治疗ADA-SCID的干细胞基因治疗药物 Strimvelis,2017年, FDA批准了基因治疗药物 Luxturna上市。据ASCGT数据,全球3633项CGT临床试验中,2024项为基因治疗管线,包括CAR-T疗法在内的基因编辑,占比为55%; 803项为不涉及基因编辑的细胞治疗管线,占比为22%。

标签: 医药医疗器械行业报告
相关文章

数据显示47.0%的人群对内分泌调理感兴趣,且64.3%已做过激素检査。性欲低下(45.9% 和性抗 拒(36.8% 是激素衰老的最直接体感,机构应将...
2026-05-06 33 医药医疗器械行业报告

针对2612名国内18-35岁的青年调研结果显示,超过八成的青年表示对于性健康知识非常了解或比较了解。显示在文化多元的氛围下,青年 的性健康意识逐渐成...
2026-05-06 28 医药医疗器械行业报告
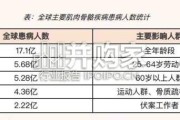
作为深耕中医药健康领域的民族企业,花红药业始终秉持“守护公众肌骨健康”的初心。我们深切体察到广大患者对于“安全止痛、便捷康复”的迫切期待,同时也关注到...
2026-05-06 21 医药医疗器械行业报告
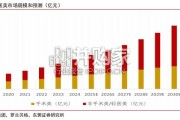
中国轻医美赛道有望成为推动行业增长的重要动力。中国医疗美容市场近年来保持较快 扩张,其中轻医美项目增长显著快于手术类项目。根据美团、罗兰贝格数据,20...
2026-05-06 19 医药医疗器械行业报告

伴随着医美产业的发展,医美注射类产品日益得 到市场关注,发展至今已经有多款产品上市并获 得市场认可,以玻尿酸、胶原蛋白、再生制剂、 肉毒素、外泌体等为...
2026-05-06 18 医药医疗器械行业报告

根据《中国卫生健康统计年鉴2022》和国家统计 局数字推算,2021年中国影像科医生配置约为 0.17人/千人,且地区分配严重不均;同时,患者 数量增...
2026-05-05 30 医药医疗器械行业报告
最新留言