心脏介入:从影像到治疗,全线布局。其中AGENT DCB球囊是美国首款/唯一治疗ISR的冠脉药球;AVVIGO+血管内超声,行业先驱,产品升级后竞争...
2026-05-10 20 医药医疗器械行业报告
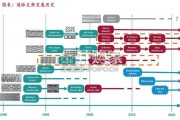
罕见病药物研发成本高,临床试验开展困难,此 前,海外的孤儿药很少考虑在中国进行申报,布 局罕见病药物研发的国内药企少之又少。我国的 罕见病患者曾长期面临“境外有药,境内无药” 的困境。为解决罕见病患者群体迫切的用药问题, 我国政府出台一系列鼓励罕见病药物研发上市的 政策举措(见图4),在丰富罕见病药物品种方面取 得了一定的进展。近5年,我国罕见疾病药物上 市数量呈现明显上升态势,但相较于美国数量仍 然较少(见图2)。 截至目前,基于《第一批罕见病目录》,199种 药物在全球上市,涉及87种罕见病;其中103种 药物在中国上市,涉及47种罕见病;其中73种药 物在中国上市并纳入医保,涉及31种罕见病(见 图3)。越来越多罕见病药物上市并纳入医保,我 国罕见病患者用药环境持续改善,但可用药物品 种与全球仍存在一定差距。对此,我国先后打造 博鳌模式和大湾区模式,可以直接引进境外已上 市的罕见病药物,提高一部分患者的用药可及性。
由于诊疗不便,药物获得存在困难等原因,罕见 病治疗比例低。大多数罕见病只能对症治疗,不 能从根本上解决患者的病痛。根据中国罕见病联 盟对33种罕见病、共20,804名患者的调研,有近 三分之一的患者目前没有接受治疗或从来未接受 过治疗。这部分人群中,又有大约一半的患者因 医药费用太贵无法负担从未进行治疗或放弃治疗。面对罕见病“境外有药,境内无药”的困局, 2018年11月至今,国家药监局先后发布三批临床 急需境外新药名单,列入名单的品种可直接提出 上市申请,CDE建立专门通道加快审评。三批临 床急需境外新药名单共计81个品种,其中罕见病 治疗药物超过一半,目录内的罕见病药物有37种。 截至目前,已有25种目录内罕见病药物上市,涉 及15种罕见病(见图5)。 罕见病药物上市进程加快,“境外有药,境内无 药”这一困境正在逐步改善,但仍有大量罕见病 药物未在国内上市。患者需要用这部分药只能通 过国外代购的方式来获得,流程复杂价格昂贵, 药品的安全性得不到保障,缺乏医生规范的临床 指导和治疗。

标签: 医药医疗器械行业报告
相关文章
心脏介入:从影像到治疗,全线布局。其中AGENT DCB球囊是美国首款/唯一治疗ISR的冠脉药球;AVVIGO+血管内超声,行业先驱,产品升级后竞争...
2026-05-10 20 医药医疗器械行业报告

展望未来十年,中国医药创新正站在新的分水岭 上。决定其能否实现新一轮跃迁的关键,在于效率能 否转化为被全球认可和定价的创新价值。从“效率高 地”迈向“...
2026-05-09 23 医药医疗器械行业报告

数据显示47.0%的人群对内分泌调理感兴趣,且64.3%已做过激素检査。性欲低下(45.9% 和性抗 拒(36.8% 是激素衰老的最直接体感,机构应将...
2026-05-06 47 医药医疗器械行业报告

针对2612名国内18-35岁的青年调研结果显示,超过八成的青年表示对于性健康知识非常了解或比较了解。显示在文化多元的氛围下,青年 的性健康意识逐渐成...
2026-05-06 46 医药医疗器械行业报告
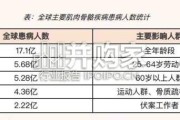
作为深耕中医药健康领域的民族企业,花红药业始终秉持“守护公众肌骨健康”的初心。我们深切体察到广大患者对于“安全止痛、便捷康复”的迫切期待,同时也关注到...
2026-05-06 25 医药医疗器械行业报告
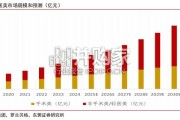
中国轻医美赛道有望成为推动行业增长的重要动力。中国医疗美容市场近年来保持较快 扩张,其中轻医美项目增长显著快于手术类项目。根据美团、罗兰贝格数据,20...
2026-05-06 22 医药医疗器械行业报告
最新留言