在带量采购常态化、支付方式改革深化及行业竞争加剧的背景下,中国医疗器械产业正处于由 “内循环”迈向“全球化”的关键拐点。国内市场的利润挤压与结构性竞争...
2026-06-10 13 医药医疗器械行业报告
2005年,国家发改委公布《国家发展改革委定价药品目录》,将血液制品列入国家发改委定价目录中,实行政府定价和政府指导价。直到 2015年,国家发改委会同国家卫计委、人社部等联合发布《关于印发推进药品价格改革意见的通知》,规定从2015年6月1日起,除麻醉 药品和第一类精神药品暂时仍由国家发改委管制,其他药品政府定价均予以取消。血液制品通过招标采购或谈判形成价格,使得血液制品 企业可以根据市场供需自主定价,在当时供不应求的市场环境下,这一政策为血液制品价格上涨打开了空间。 在市场力量的主导下,采浆量从2015年的5846万吨迅速提升至2016年的7200吨,增长23.2%。近两年受渠道库存积压影响,行业采浆量 增速有所放缓。 2016年,卫计委发布《关于促进单采血浆站健康发展的意见》(国卫医发〔2016〕66号),要求严格新增单采血浆站设置审批,再次强 调按照向研发能力强、血浆综合利用率高、单采血浆站管理规范的血液制品生产企业倾斜原则,依法做好单采血浆站的审批工作。这也代 表了未来国内血液制品的发展方向必将是研发驱动、管理驱动的精细化道路。
血液制品(尤其是静丙和白蛋白)在新冠的预防和治疗发挥了重要作用。疫情期间,除血液制品企业加紧生产供货外,国家药监局也“对 临床急需的静注人免疫球蛋白(pH4)、人血白蛋白等血液制品,在企业自检时同步进行批签发“,使得2020Q1相关品种的批签发量均 有大幅增长,其中静丙同比增长96%、白蛋白同比增长75%。 由于静丙和特免在生产中是互斥的,除乙免外,特免类品种2020Q1增速均有一定下滑。乙免2020Q1同比高速增长160%,主要由于 2019Q1基数较低。 因子类产品中,纤原批签发进一步下滑,2020Q1同比减少8%;八因子和PCC适应症明确,终端需求刚性,批签发增速则均大幅提升。

标签: 医药医疗器械行业报告
相关文章

在带量采购常态化、支付方式改革深化及行业竞争加剧的背景下,中国医疗器械产业正处于由 “内循环”迈向“全球化”的关键拐点。国内市场的利润挤压与结构性竞争...
2026-06-10 13 医药医疗器械行业报告

矛盾一:招人越来越难。年轻人对”按摩技师”职业的认同感持续走低。郑远元之所以能维持74,645名员工的庞大团队,核心在于其独特的"从贫困山区...
2026-06-09 22 医药医疗器械行业报告

集采推动国内胰岛素渗透率提升,市场规模自 2024 年起重回增长通道。胰岛素首轮集采中选结果于 2022 年 5 月开始 实施,对国内胰岛素市场产生深...
2026-06-09 18 医药医疗器械行业报告
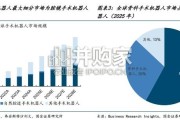
随着精准医疗理念的深入与微创外科技术的普及,手术机器人正逐步重塑现代外科手术的 范式,成为全球医疗器械领域最具增长潜力的细分赛道之一。作为集医学、生物...
2026-06-09 18 医药医疗器械行业报告
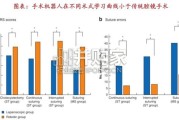
手术机器人是指在医疗手术中辅助医生操作的智能机器人系统,由医生控制台、机械臂系统和成像系统等组成。 通常由四只机械臂模拟医生微创手术工作,三维电子腹腔...
2026-06-08 34 医药医疗器械行业报告

本次调研显示,56.0%的受访者来自公立三甲医院,且85.1%为执业超过10年的资深医务人 员。这个样本特征非常关键,它意味着当前医疗AI的积极使用者...
2026-06-04 29 医药医疗器械行业报告
最新留言